Aktuelle Forschung
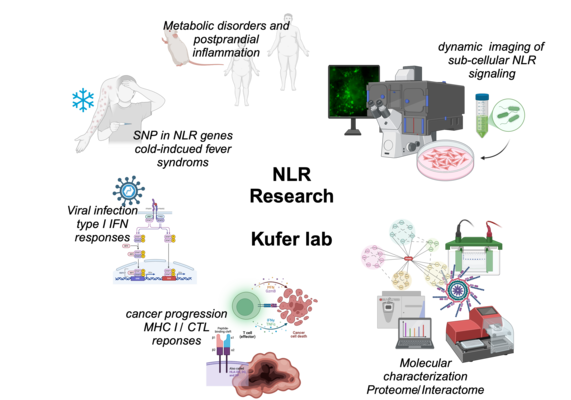
Schwerpunkt der Forschungsarbeiten der Fachgruppe Immunologie ist die molekulare und zellbiologische Charakterisierung von Proteinen der nucleotide-binding domain, leucine-rich repeat containing-Familie (NLR) im Menschen und in Mausmodellen.
NLRs bilden eine Familie von 22 ATPasen mit hoher physiologischer Relevanz. Während die Funktion einiger NLRs im Menschen derzeit immer noch nicht gut verstanden ist, konnte für mehrere Mitglieder essenzielle Funktionen als Mustererkennungsrezeptoren in der angeborenen Immunantwort für Pathogene und Zellschädigung und der daraus resultierenden Induktion pro-inflammatorischer Zytokine belegt werden. Die medizinische Relevanz von NLRs ist durch Erbkrankheiten belegt, denen Polymorphismen in NLR-kodierenden Genen zugrundeliegend. Beispiele sind das Bare-Lymphocyte Syndrom, das Blau-Syndrom, genetische Prädisposition für Morbus Crohn und Familial Cold Autoinflammatory Syndromes (FCAS) (Kufer and Sansonetti 2011, Nat Immunol.).
Der Fokus unserer Forschungsarbeiten liegt hierbei auf der Entschlüsselung der Funktion dieser Proteine in der angeborenen Immunität, der Regulation immunologischer Vorgänge und NLR-assoziierter Erkrankungen. Dies erfolgt in engen Kooperationen mit nationale und eine Reihe internationaler Kolleginnen und Kollegen (Sherbrooke University, Canada; Monash Medical Research, Melbourne, Australia; University of Lille, Frankreich).
Zudem interessieren wir uns für die Funktionen von NLR-Proteinen bei maligner Entartung. Unsere Arbeitsgruppe konnte NLRC5 als Regulator der MHC Klasse I Gene identifizieren (Neerincx et al, 2012, JI ). Laufende Projekte zielen u.a. auf die Entwicklung von Methoden zur Expression von NLRC5 in der Tumortherapie ab. In diesem Kontext ist zu erwähnen, dass wir auch Projekte zur Analyse der Funktion von NLRP11 verfolgen, welches sehr hoch in einigen B-Zell Lymphomen exprimiert wird (Ellwanger et al. 2018 JBC). Für NOD1 konnten wir zeigen, dass dies zusammen mit dem Protein HAX-1 bei der Zellmigration von Tumorzellen eine wichtige Rolle spielt (Hezinger et al. 2023, FEBS Journal).
Weitere Aspekte unserer Forschungsarbeiten betreffen die Analyse von krankheitsassoziierten Polymorphismen in NLR-Genen und deren molekulare Funktion. Dies konnten wir z.B. an Mutationen im NLRP12 in Kontext der Immunabwehr in Darm zeigen (Normand et al. 2018 Nat.Comm.). Laufende Arbeiten befassen sich mit der Aufklärung der bisher immer noch wenig verstandenen Aktivierung dieser Proteine und deren Zellbiologie. In Kollaboration mit der Universität Bonn konnten wir so zur Identifikation einer neuen Funktion von NLRP10 als Inflammasom beitragen (Próchnicki et al. 2023 Nat. Immunol.). Zudem konnten wir Veränderungen der sub-zellulären Lokalisation von RIPK2 nach NOD1/2 Aktivierung und deren molekulare Grundlagen aufklären (Ellwanger et al. 2019, Life Sci Alliance, Steinle et al. 2021, J Cell Sci).
Ein besonderer Schwerpunkt unsers Forschungsportfolio ist die immunologische Forschung im Kontext der Ernährung und von metabolischen Störungen. Als Partner im EU-geförderten Projekt RESIST-PP (EU HDHL-NUTRIMMUN) untersuchen wir aktuell die postprandiale Immunantwort in gesunden und übergewichtigen Personen und im BMBF-geförderten Projekt INDICATE-FH die Immunreaktionen im Darm bei Nahrungsmittelunverträglichkeit.
Wir bearbeiten vor allem Funktionen der angeborenen Immunreaktionen im Kontext metabolischer Erkrankungen. NLR-Proteine spielen hier eine wichtige Rolle (siehe hierzu unseren Übersichtsartikel: Bauer et al. 2023, Int J Mol Sci.), so konnten wir in einem Hochfett-Diät Modell in der Maus zeigen, dass NLRC5 eine neue Funktion bei Übergewicht hat (Bauer et al. 2023, iScience).